Рецензируемый «Российский паразитологический журнал» издается с 2007 года. «Российский паразитологический журнал» предназначен для научных исследователей в области медицинской, ветеринарной и фитопаразитологии из различных стран мира: России, стран СНГ, Ближнего и Дальнего Зарубежья. Журнал является Международным научно-практическим изданием по фундаментальным и прикладным вопросам паразитологии и единственным в России изданием по ветеринарной паразитологии и фитогельминтологии.
Журнал издается 4 раза в год (ежеквартально) тиражом 500 экз. и является подписным изданием. Подписной индекс в каталоге «Почта России» ПН282.
Журнал зарегистрирован в Министерстве Российской Федерации по делам печати, телерадиовещания и средств массовых коммуникаций 12 января 2007 года (Свидетельство ПИ № ФС77-26864 от 12.01.07 г.). Перерегистрирован по причине изменения названия учредителя 19 октября 2018 года (Свидетельство ПИ № ФС77-74051 от 19.10.18 г.).
«Российский паразитологический журнал» включен в список Russian Science Citation Index (RSCI) на платформе Web of Science, входит в ядро РИНЦ и в Перечень рецензируемых научных изданий ВАК Минобрнауки РФ, в которых должны быть опубликованы основные научные результаты диссертаций на соискание ученой степени кандидата наук, на соискание ученой степени доктора наук. Журнал является членом Комитета по этике научных публикаций, Ассоциации научных редакторов (АНРИ) и CrossRef.
УЧРЕДИТЕЛЬ
ФГБНУ ФНЦ ВИЭВ РАН
ИЗДАТЕЛЬ
ВНИИП – филиал ФГБНУ ФНЦ ВИЭВ РАН
РЕДАКЦИЯ ЖУРНАЛА
ВНИИП – филиал ФГБНУ ФНЦ ВИЭВ РАН
117218, Россия, г. Москва, ул. Б. Черемушкинская, 28
Текущий выпуск
ФАУНА, МОРФОЛОГИЯ И СИСТЕМАТИКА ПАРАЗИТОВ
Цель исследования – сравнительный анализ гельминтофауны водяного ужа серой и черной морфы, обитающих в Нижнем Поволжье.
Материалы и методы. Методом полного гельминтологического вскрытия исследованы 32 особи серых и 41 особь черных водяных ужей Natrix tessellata из трех местообитаний Астраханской области, отловленных в 2004, 2005, 2008 гг. Обработку паразитологического материала проводили стандартными методами. Статистический анализ выполняли с использованием индексов Шеннона, Жаккара, Серенсена, доминирования Ковнацкого, критерия Манна-Уитни.
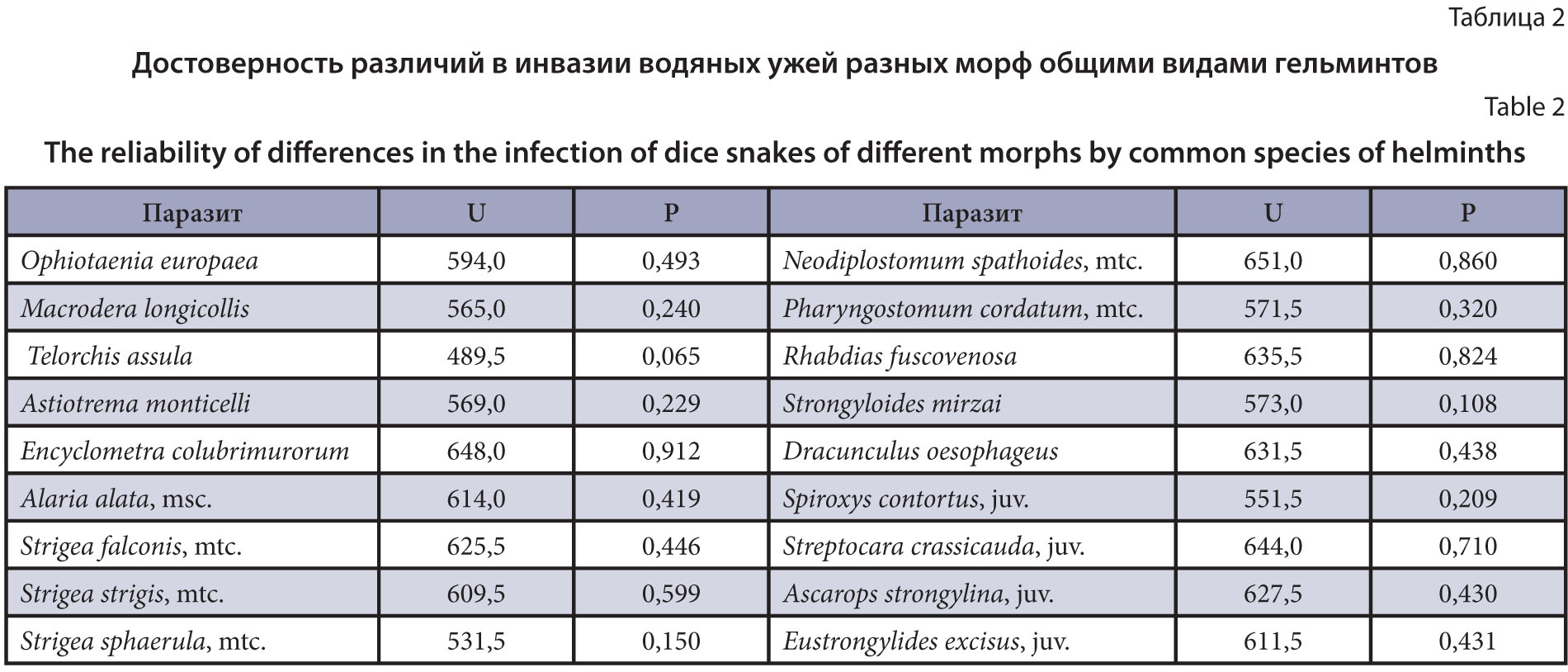
Результаты и обсуждение. Проведен сравнительный анализ гельминтофауны водяного ужа серой и черной морфы. Всего у исследованных водяных ужей отмечен 21 вид паразитических червей: Cestoda – 1, Trematoda – 11, Nematoda – 8, Acanthocephala – 1. Все эти виды гельминтов обнаружены у серых ужей. У N. tessellata черной окраски зарегистрировано 18 видов паразитов. Только у ужей серой морфы встречены Paralepoderma cloacicola, Camallanus lacustris и Centrorhynchus aluconis. Анализ общей зараженности гельминтами водяных ужей разной морфы не выявил достоверных различий, как и попарное сравнение инвазии рептилий общими видами паразитов. Установлено, что в фауне гельминтов серых и черных N. tessellata состав и степень доминирования паразитов различается. Сравнение гельминтофауны водяных ужей серой и черной морфы как в качественном, так и количественном отношении, показало высокую степень сходства. Разнообразие паразитофауны серых и черных N. tessellata находится примерно на одном уровне. Сходный состав гельминтов водяных ужей разной окраски указывает на сходство их топических и трофических ниш. Относительно большая зараженность серых водяных ужей гельминтами вероятно связана с различиями в физиологии. Установлено, что в формировании гельминтофауны водяного ужа принимают участие обе морфы N. tessellata.
ЭПИЗООТОЛОГИЯ, ЭПИДЕМИОЛОГИЯ И МОНИТОРИНГ ПАРАЗИТАРНЫХ БОЛЕЗНЕЙ
Цель исследований – оценить влияние системы содержания, сезона и погодных условий на число яиц желудочнокишечных нематод в фекалиях у лошадей Амурской области Дальнего Востока России в 2021–2024 гг.
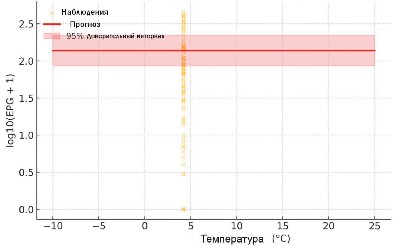
Материалы и методы. Всего собрано 1494 проб фекалий индивидуально от 212 лошадей, содержавшихся на постоянном выпасе (три фермы) или в стойлах с ежедневным выгулом (четыре фермы). Яйца Strongylata spp., Parascaris equorum и Oxyuris equi подсчитывали по методу Мак-Мастера. Среднемесячные значения температуры воздуха, относительной влажности и количества осадков были получены от ФГБУ «Гидрометцентр России». Число яиц было преобразовано в логарифмическую шкалу [log₁₀(EPG + 1)]. Предварительные связи изучены с помощью ранговой корреляции Спирмена; детерминанты выделения яиц стронгилят оценены с помощью обычной регрессии наименьших квадратов с кластерно-устойчивыми (HC1) стандартными ошибками для фактора «ферма» (n = 7).
Результаты и обсуждение. Нематоды Strongylata spp. были практически повсеместны (99% лошадей), тогда как P. equorum и O. equi встречались у 24% и 8% лошадей, соответственно. Выпас на пастбище увеличил логарифмическую FEC стронгилят на 0,29±0,06 (в 1,9 раза; Р < 0,001) и осенний отбор проб на 0,22±0,05 (в 1,6 раза; Р < 0,001) по сравнению с весенним. Каждый 1оC повышения среднемесячной температуры добавлял 0,035±0,009 логарифмических единиц (Р < 0,001). Влажность и количество осадков не показали независимого влияния после корректировки. Не было обнаружено значимой зависимости от погодных условий для P. equorum или O. equi. Таким образом, непрерывный выпас в сочетании с теплыми погодными условиями является основным фактором риска заражения стронгилятами. Для улучшения контроля и сокращения ненужных зимних обработок рекомендуется проводить стратегическую дегельминтизацию в апреле и сентябре в сочетании с селективной терапией.
Цель исследований – разработать сезонную прогностическую модель численности комаров (сем. Culicidae) на территории Калужской области на основе методов анализа временных рядов с учетом климатических факторов, обеспечивающую точность прогноза не менее 85% для оперативного планирования противоэпидемических мероприятий.
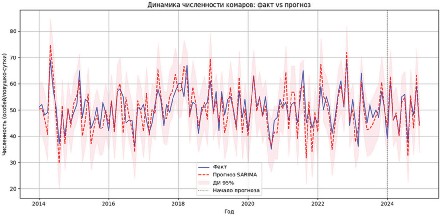
Материалы и методы. В ходе исследования динамики численности комаров на территории Калужской области за 2014–2024 гг. применен комплексный подход, сочетающий полевые наблюдения, статистический анализ и математическое моделирование. Параллельно анализировали климатические параметры (среднемесячные температуры, количество осадков, влажность воздуха). Использован метод моделирования с применением временных рядов.
Результаты и обсуждение. Построена прогностическая модель численности комаров в Калужской области на 2024 г. с использованием сезонной модели SARIMA. Полученные результаты демонстрируют надежность прогноза: средняя абсолютная процентная ошибка составляет 7,9%, что означает отклонение прогноза от фактических значений менее чем на 8%, в среднем. Среднеквадратическая ошибка в 147,2 особи показывает, что в абсолютных значениях прогнозные данные могут отличаться от реальных примерно на 150 особей при средней численности популяции около 1800–2500 экз. Эти показатели свидетельствуют о высокой достоверности модели и ее применимости для практического использования. Полученные результаты имеют важное практическое значение для планирования своевременных обработок территорий, оптимизации работы эпидемиологического надзора, распределения ресурсов для борьбы с переносчиками заболеваний и информирования населения о периодах повышенной активности комаров.
Цель исследований – изучение распространения таких био- и геогельминтов как Spirometra erinaceieuropaei, Trichinella spp., Тохосаrа spp., Ascaris spp. на территории Центрального Черноземья (на примере Курской и Орловской областей).
Материалы и методы. С апреля по ноябрь 2024 года получена 321 положительная проба – воды, ливневых стоков, почвы, донных отложений. На территории Курской области исследования проводили в Курском, Железногорском, Дмитриевском и Солнцевском районах, на территории Орловской области – в Дмитровском районе. Воду исследовали, используя аппарат «ПробоКонГ». Отбор проб почв, поверхностного стока и донных отложений проводили по МУК 4.2.2661-10, вскрытие млекопитающих проводили по К. И. Скрябину (1938). Электронные карты составляли в среде ГИС «Аксиома», используя ПО «Google My Maps», «Яндекс-карты» и «Навител».
Результаты и обсуждение. Установлено широкое распространение спарганоза, трихинеллеза, аскаридоза и токсокароза на территориях исследуемых районов. Пробы, взятые из открытых водных источников, показали среднюю степень контаминации яйцами S. erinaceieuropaei – 5,4%, причем наименьшее количество инвазионного материала наблюдали на территории Курского района Курской области – 1,9%, наибольшее – в Железногорском и Солнцевском – по 6,6%. Во многих пробах почвы обнаружены инвазионные яйца геогельминтов – Тохосаrа spp. и Ascaris spp. Яйца геогельминтов найдены на территориях Курского и Железногорского районов Курской области, а также Дмитровского района Орловской. Результаты объясняются наличием агропредприятий на территории исследуемых районов, а также значительной антропогенной нагрузкой. При проведении гельминтологических вскрытий грызунов на территории Солнцевского района Курской области были обнаружены серые крысы (Rattus norvegicus (Berkenhout, 1769)), зараженные капсулами Trichinella spp.
Цель исследований – получить сведения о современном состоянии зараженности крупного рогатого скота фасциолезом в различных хозяйствах Республики Дагестан.
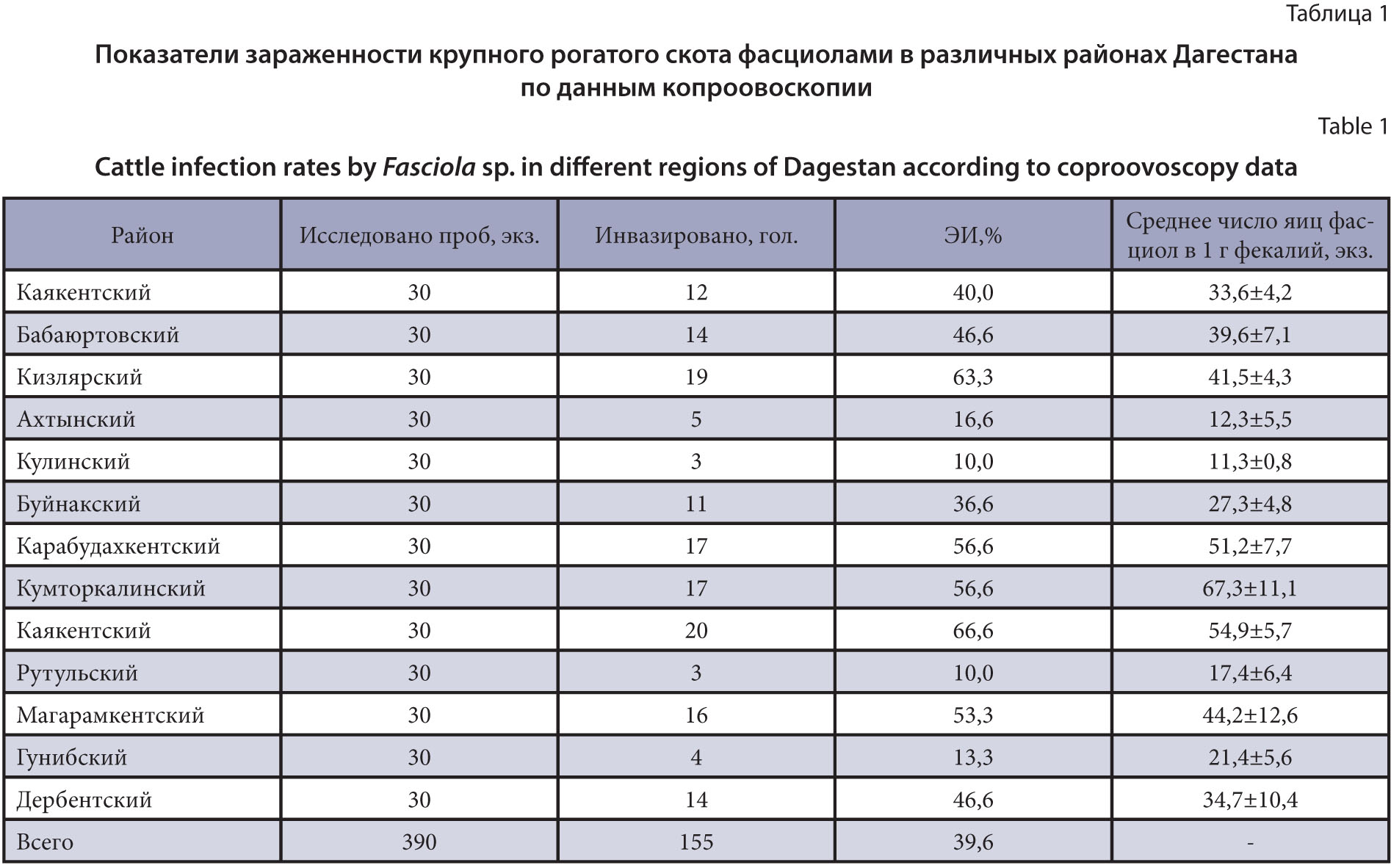
Материалы и методы. Исследования проводили с марта по июль 2025 г. в различных хозяйствах Республики Дагестан на всех высотных уровнях. Пробы фекалий от 390 голов крупного рогатого скота исследовали методом флотации с использованием счетной камеры ВИГИС в лаборатории по изучению инвазионных болезней сельскохозяйственных животных и птиц Прикаспийского ЗНИВИ. Исследование внутренних органов 287 туш проводили на убойных пунктах г. Махачкалы путем осмотра и вскрытия печени, а также желчевыводящих путей. Результаты исследований подвергали статистической обработке с использованием компьютерного пакета «Биометрия».
Результаты и обсуждение. По результатам исследований, проведенных в период с марта по июль 2025 г., установлена распространенность фасциолеза крупного рогатого скота в республике. По данным копроовоскопии средняя зараженность крупного рогатого скота составила 39,6%, при послеубойном осмотре внутренних органов – 41,1%. Инвазия распространена повсеместно в различных районах Дагестана. Наблюдается рост заражения от высокогорных районов к низменным, чему способствует большее число открытых водоемов, рек и заливных лугов, расположенных ближе к морю, где обитают промежуточные хозяева фасциол – моллюски. Полученные данные указывают на необходимость изучения эпизоотической ситуации, усиления борьбы с данной инвазией на всех уровнях.
БИОХИМИЯ, БИОТЕХНОЛОГИЯ И ДИАГНОСТИКА
Цель исследований – отработать метод пробоподготовки, используя расходные материалы (лизис-буферы) российского производства, для изучения белкового профиля санитарно-значимых гельминтов промысловых рыб методом времяпролетной масс-спектрометрии с лазерной десорбцией/ионизацией (MALDI-TOF).
Материалы и методы. Для работы были отобраны 98 экз. гельминтов от трех видов рыб: половозрелые цестоды Triaenophorus nodulosus из кишечника щуки (Esox lucius), плероцеркоиды (личинки) цестод Diphyllobothrium ditremum из стенки желудка и кишечника ряпушки европейской (Coregonus albula), личинки нематод Eustrongylides excisus из мышечной ткани и печени окуня обыкновенного (Perca fluviatilis). Ихтиологический материал был получен с помощью пассивных орудий лова (сети) в период с января по август 2025 года и доставлен в лабораторию в замороженном виде. В лабораторных условиях проводили вскрытие рыб, осмотр мышечной ткани и внутренних органов под бинокулярным микроскопом Motic SMZ-171T. Для видовой идентификации паразитов использовали определители паразитов пресноводных рыб фауны СССР Гусева (1985) и Авдеева (1987). Фотодокументацию выполняли на микроскопе Zeiss AxioImager Z.1. Пробоподготовку (экстракцию) гельминтов проводили согласно патенту N RU 2768162 C1 «Способ подготовки половозрелых особей нематод для идентификации методом MALDI TOF масс-спектрометрии» (2022). Масс-спектрометрию гельминтов выполняли на масс-спектрометре MALDI (Microflex, Bruker Germany).
Результаты и обсуждение. На сегодняшний день в Российской Федерации имеется необходимость в разработке, верификации и внедрении в практическую деятельность испытательных лабораторий рабочих протоколов метода MALDI-TOF MS для диагностики инвазий рыб, используемых для пищевых целей, и создания единой референсбиблиотеки спектров белков гельминтов, встречающихся на территории России. Однако, метод пробоподготовки (экстракции) гельминтов не отработан и не разработан стандартный операционный протокол для проведения диагностического исследования гельминтов методом времяпролетной масс-спектрометрии. Нами предприняты исследования по отработке метода пробоподготовки (экстракции) гельминтов с использованием расходных материалов и реактивов российского производства. В результате проведенных нами исследований был отработан протокол пробоподготовки и получен 41 масс-спектр.
Цель исследований – определение видовой принадлежности плероцеркоидов Dibothriocephalus spp. из летней кеты Oncorhynchus keta, отловленной в реке Амур, на основании анализа фрагмента гена первой субъединицы цитохром с-оксидазы (COX1) митохондриальной ДНК.
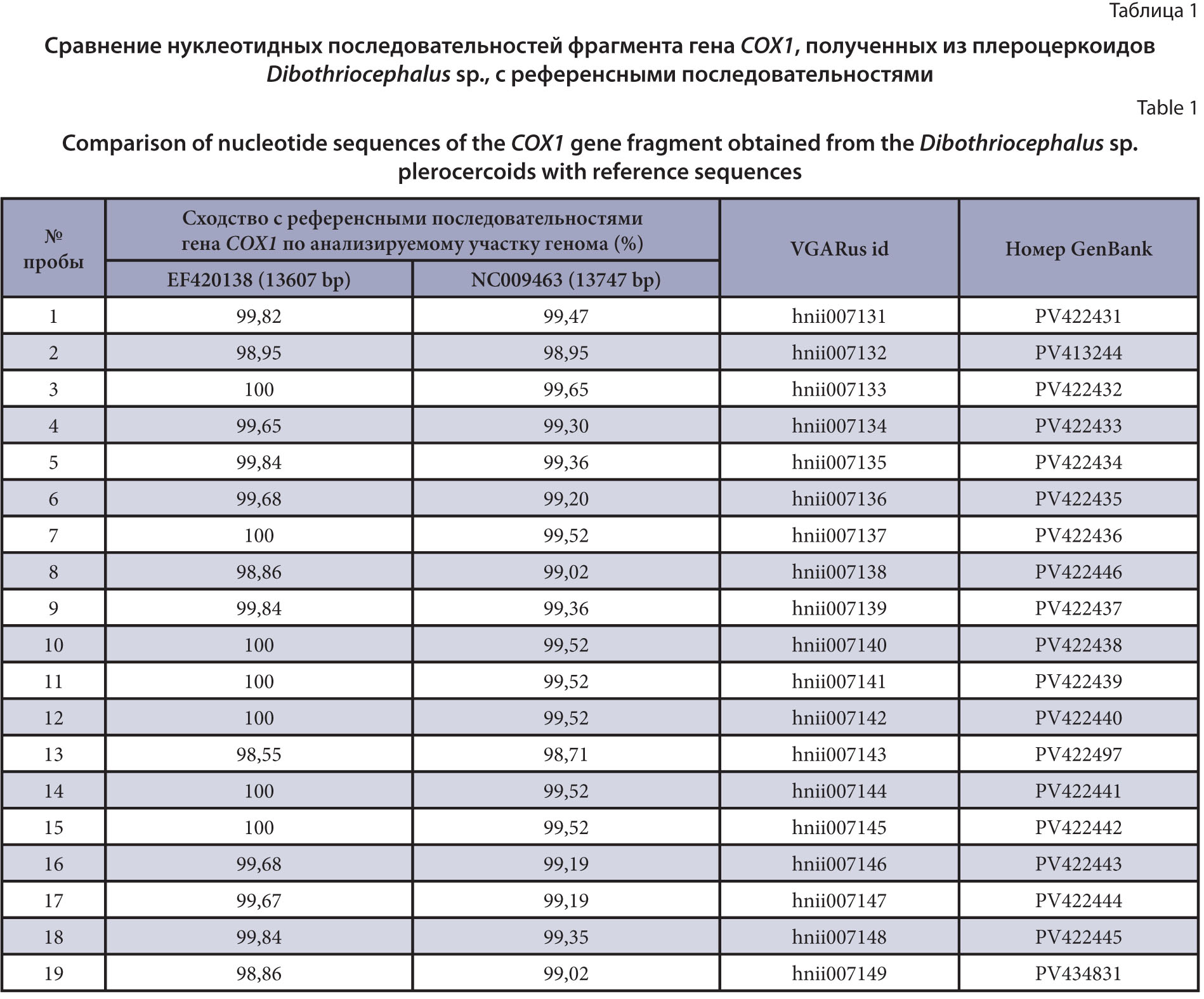
Материалы и методы. Методом неполного гельминтологического вскрытия изучены 64 экз. кеты летней (Oncorhynchus keta), выловленной в р. Амур на территории Ульчского района Хабаровского края. Из фрагментов обнаруженных плероцеркоидов Dibothriocephalus spp. проводили экстракцию ДНК, амплификацию фрагмента гена, кодирующего первую субъединицу цитохром с-оксидазы (COX1) митохондриальной ДНК D. nihonkaiensis. Продукты амплификации секвенировали по Сэнгеру. Полученные нуклеотидные последовательности анализировали с помощью онлайн-алгоритма BLAST.
Результаты и обсуждение. Плероцеркоиды типа F были обнаружены у 38 особей кеты летней O. keta. Полученные методом секвенирования нуклеотидные последовательности фрагмента гена COX1 (579 п.о.) показали сходство на 98,55–100% по анализируемому участку с референсными последовательностями D. nihonkaiensis, зарегистрированными в GenBank. В результате проведённых исследований подтверждена инвазированность кеты летней O. keta, выловленной в р. Амур, возбудителем дифиллоботриоза Dibothriocephalus nihonkaiensis.
Цель исследований – определить оптимальные временные и температурные параметры при выделении нематод Bursaphelenchus xylophilus вороночным методом Бермана из древесины сосны Pinus sylvestris L.
Материалы и методы. Фрагменты ствола P. sylvestris длиной 22–25 см, выпиленные из 15-летнего визуально здорового дерева сосны были заражены сосновой стволовой нематодой B. xylophilus и их инкубировали в течение 45 сут в термостате при температуре 27 °С. При бурении дрелью зараженных нематодами бревен получали опилки, из которых сформировали единый образец древесного субстрата. Для выделения нематод из древесного образца использовали вороночный метод Бермана. Опыт включал четыре варианта по 8 образцов. Численность нематод определяли через 6, 24 и 48 ч при температуре 18 и 25 °С. Данные обрабатывали в среде MS Excel.
Результаты и обсуждение. Установлено, что около 80% нематод выделяется в течение первых 24 ч. Этот срок является оптимальным при проведении фитогельминтологического анализа. Число выделенных нематод в последующие сутки составило около 20%. Изменение температуры в пределах 18–25 °С влияло на степень экстракции нематод из древесного субстрата, но не всегда существенно. Численность выделенных нематод в различных воронках, полученных из одного смешанного образца, существенно различалась, что объясняется агрегированностью их распределения в древесном субстрате.
ПАТОГЕНЕЗ, ПАТОЛОГИЯ И ЭКОНОМИЧЕСКИЙ УЩЕРБ
Цель исследований – изучение клинико-морфологических и биохимических показателей периферической крови собак с подтвержденным диагнозом на лейшманиоз в условиях Республики Кипр.
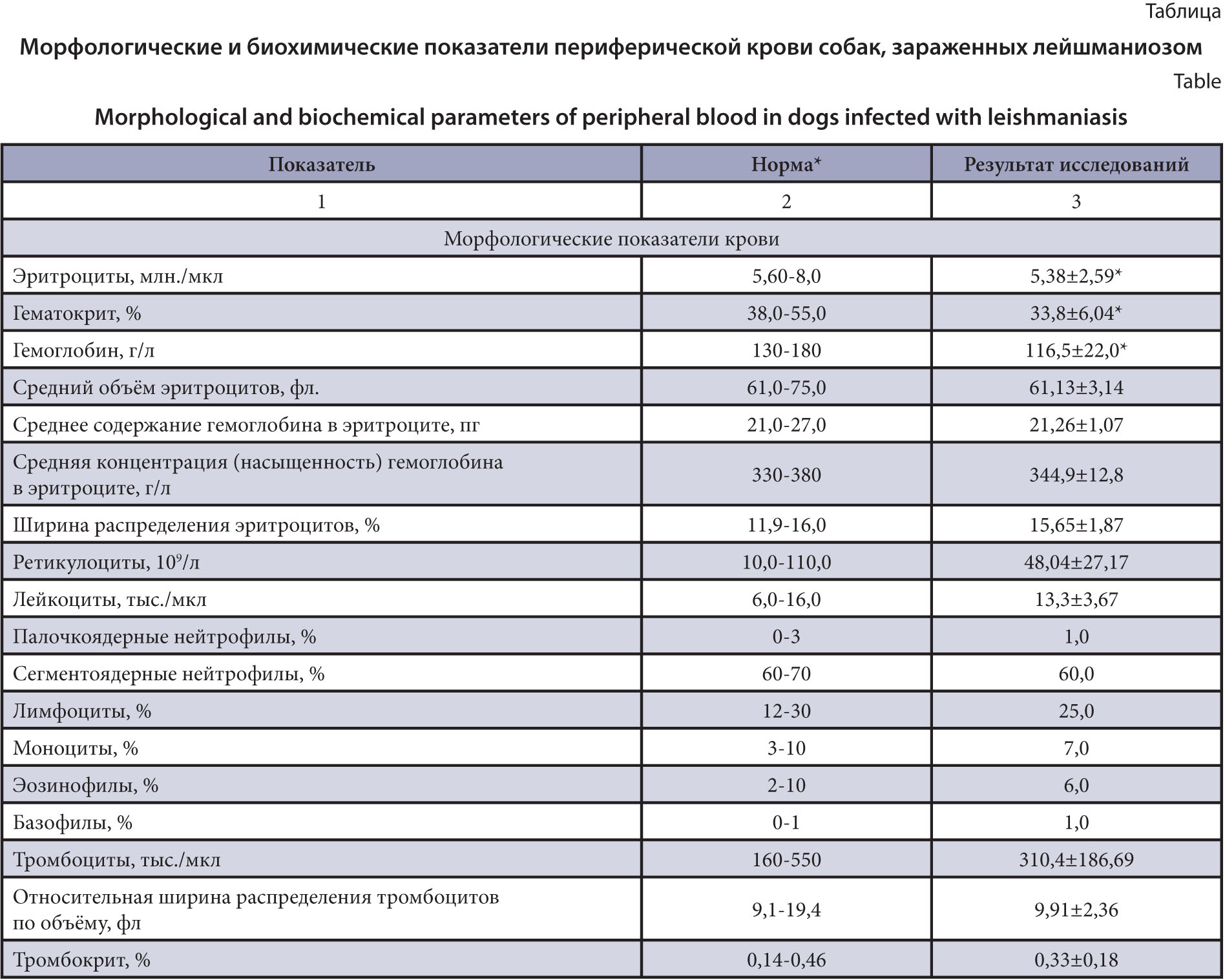
Материалы и методы. Изучали морфологические и биохимические показатели крови 8 собак охотничьих пород массой 15–23 кг, содержащихся на территории частных домовладений в вольерах или на улице в городе Пафос (Республика Кипр), зараженных лейшманиозом. Диагноз на наличие антител к паразиту устанавливали с помощью теста SNAP (IDEXX, США) на основе иммуноферментного анализа. Для клинического анализа крови использовали гематологический анализатор IDEXX ProCyte Dx, а биохимические исследования крови собак проводили на анализаторе IDEXX Catalyst Dx.
Результаты и обсуждение. Установлено, что у большинства собак, зараженных лейшманиозом, есть как общие отрицательные изменения в клетках крови, системах организма и органах-мишенях, так и индивидуальные изменения. Из общих изменений в периферической крови собак отмечают эритроцитопению, снижение содержания гемоглобина, повышение уровней креатинина, мочевины и фосфора, что может свидетельствовать о развитии острой почечной недостаточности, также повышение активности аланинаминотрансферазы и щелочной фосфатазы.
ЛЕЧЕНИЕ И ПРОФИЛАКТИКА
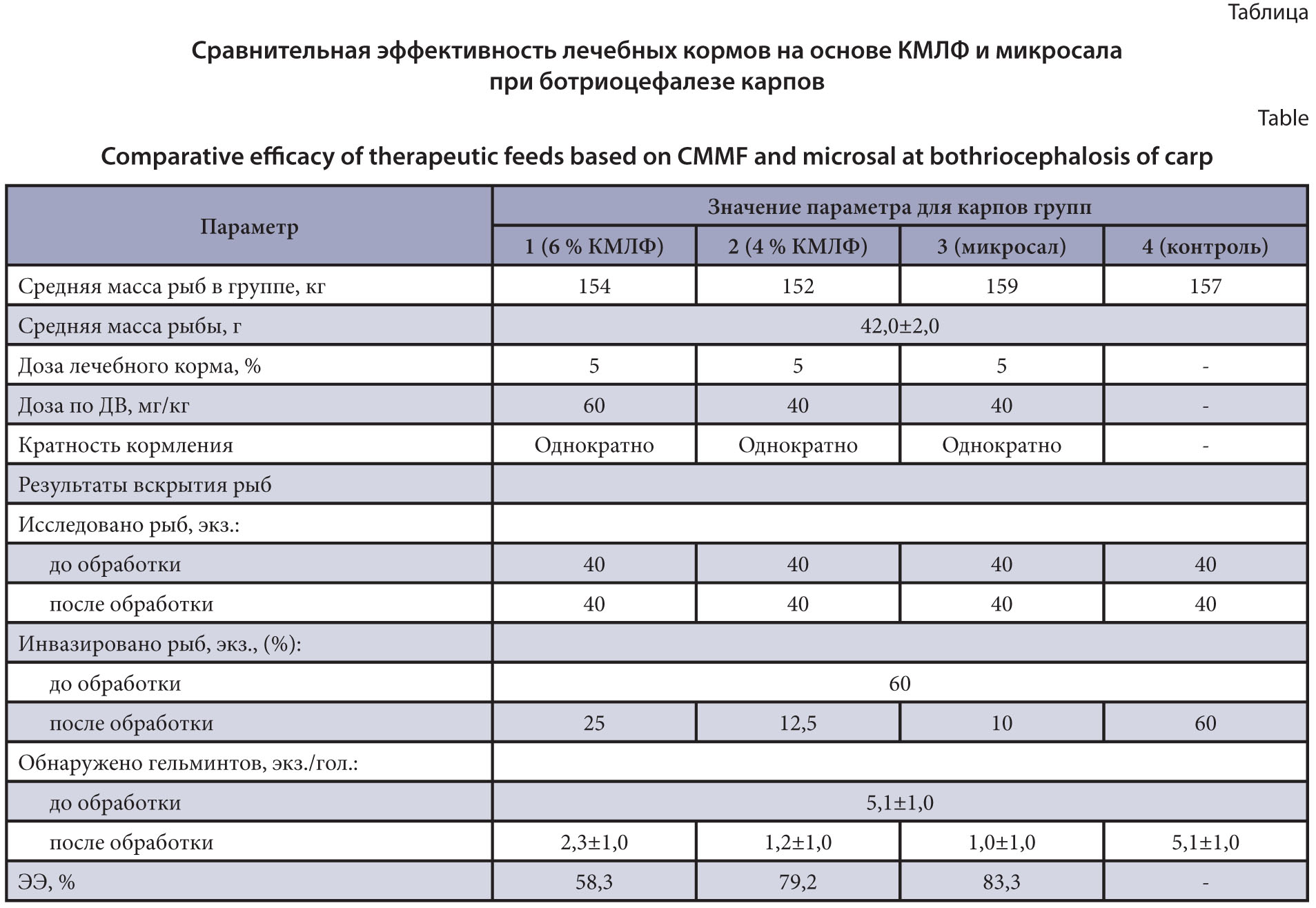
Цель исследований – сравнительное испытание комбинированных микронизированных лекарственных форм на основе бензимидазолов и никлозамида при ботриоцефалезе карпов в условиях производства.
Материалы и методы. Ранее разработана рецептура двух лекарственных форм на основе альбендазола с никлозамидом и фенбендазола с никлозамидом. Наработаны лабораторные партии лечебных кормов с комбинированными микронизированными лекарственными формами, установлена степень инвазированности рыб ботриоцефалюсами в вегетационный период и эффективность комбинированных микронизированных лекарственных форм при ботриоцефалезе карпов согласно общепринятым методикам. Дана оценка эффективности применения комбинированных микронизированных лекарственных форм в условиях производства.
Результаты и обсуждение. При сравнительном испытании в условиях производства двух комбинированных микронизированных лекарственных форм в составе лечебных гранулированных комбикормов при ботриоцефалезе карпов наиболее эффективным оказался лечебный корм с 4%-ной комбинированной микронизированной лекарственной формой на основе альбендазола и никлозамида при однократной даче при 5%-ной норме кормления. Данная лекарственная форма показала эффективность, близкую к базовому препарату (микросалу), который используется в настоящее время для терапии ботриоцефалеза карповых рыб.
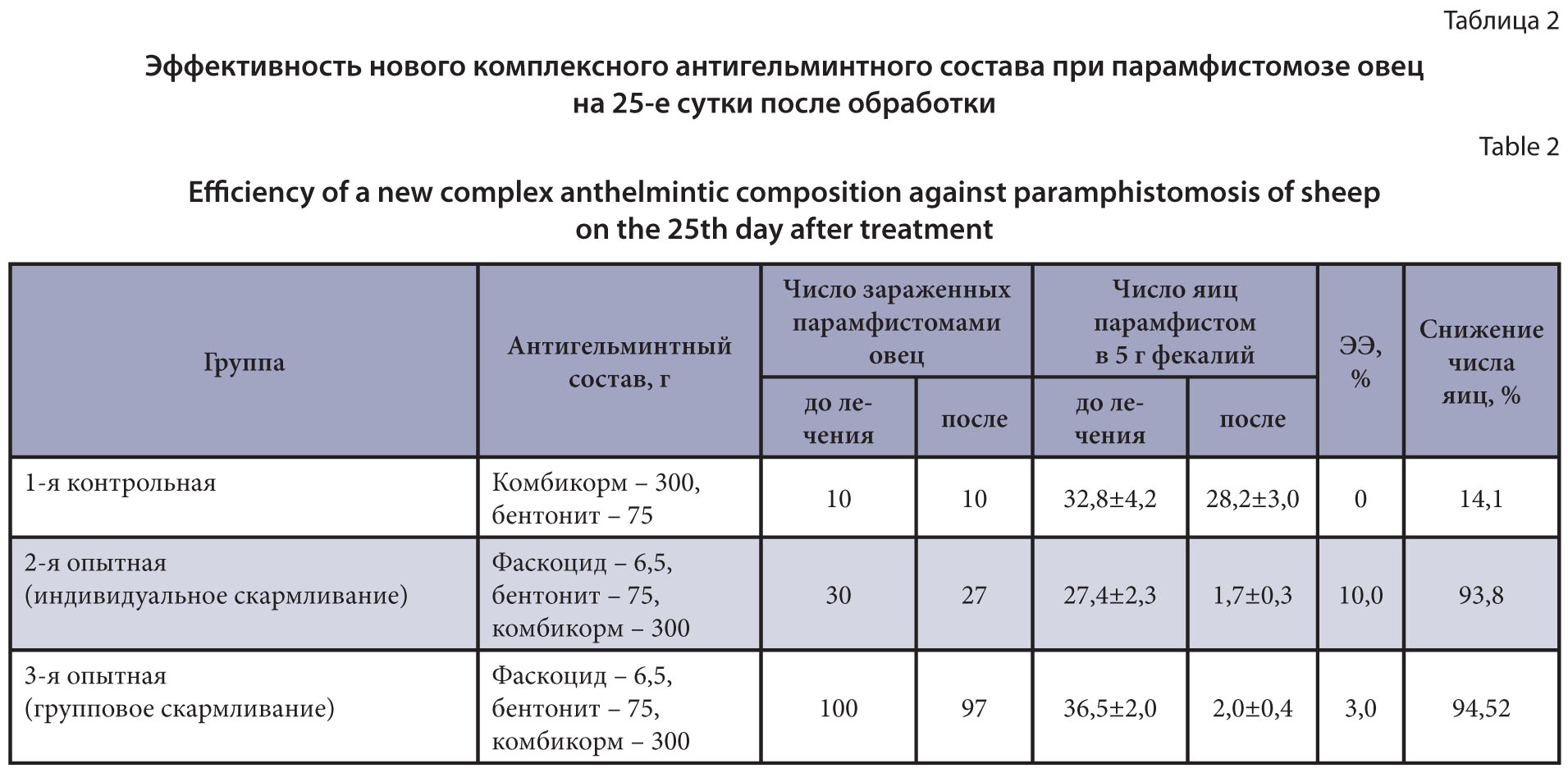
Цель исследований – разработка группового способа лечения парамфистомоза овец фаскоцидом гранулятом с микронизированным порошком бентонита размером частиц 25–60 мкм с концентрированным кормом.
Материалы и методы. Исследования проводили в 2025 г. в лаборатории по изучению инвазионных болезней сельскохозяйственных животных и птиц. Объектом исследований служили 140 овец в возрасте 1-4 лет, массой тела 55–65 кг породы дагестанский горный меринос. Исследовали пробы фекалий животных подопытных групп, а также комплекты желудочно-кишечного тракта овец, поступивших на убойный пункт Шамхал-Тюбе. Разработку и испытание способа лечения парамфистомоза путем группового скармливания фаскоцида гранулята в смеси с микронизированным порошком природного минерала бентонита размером частиц 25–60 мкм с концентрированным кормом проводили на базе хозяйства «Агрофирма Чох» Гунибского района, на зимних пастбищах Кумторкалинского района.
Результаты и обсуждение. Результаты исследования показали высокую эффективность комбинированного препарата фаскоцид гранулят + микронизированный порошок бентонита при парамфистомозе овец с концентрированным кормом – 94,52% методом группового скармливания. Данный способ применения антигельминтного средства, особенно в условиях отгонного типа ведения животноводства, обладает рядом преимуществ, таких как снижение производственного стресса, материальных затрат и сокращение времени на проведение профилактических мероприятий.
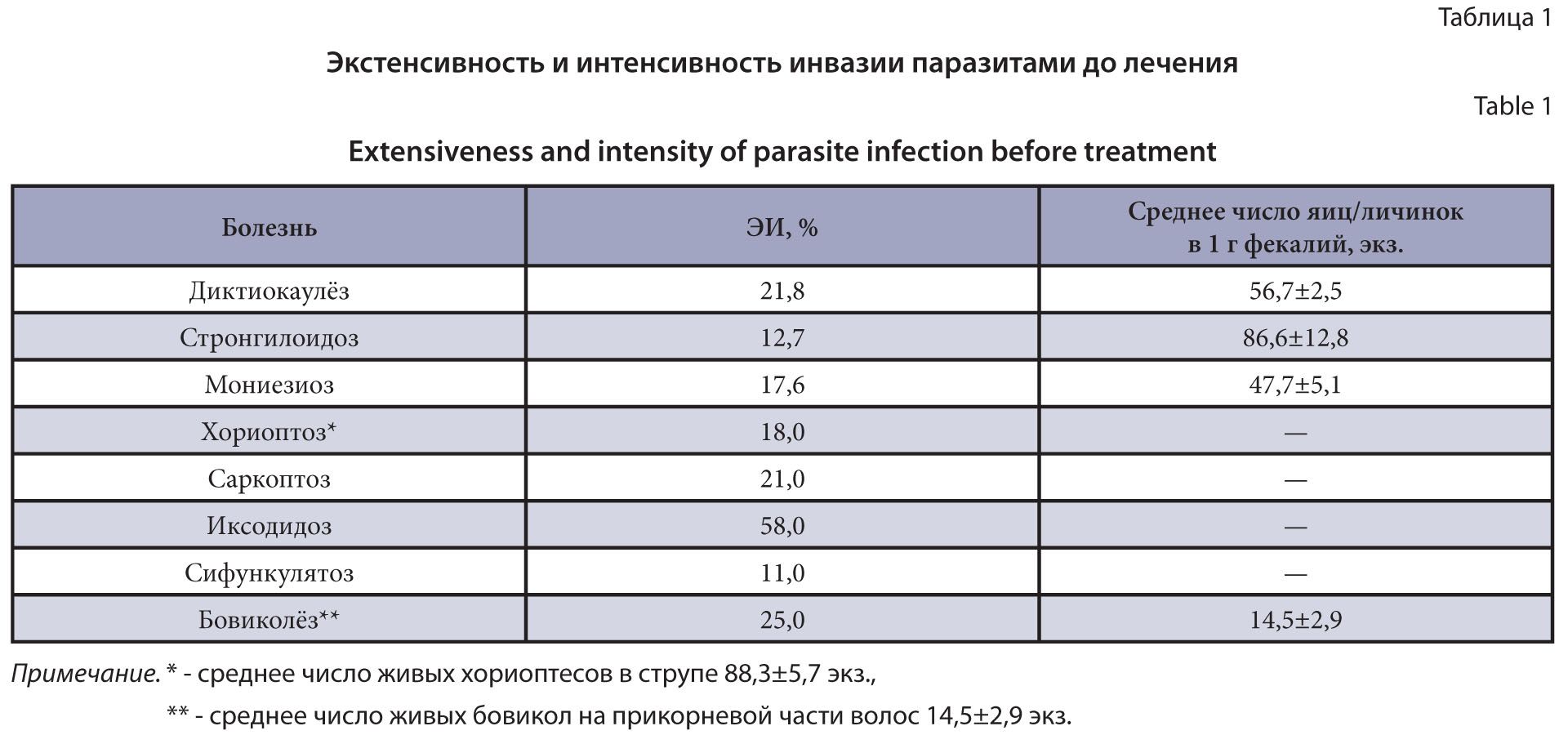
Цель исследований – изучить терапевтическую эффективность и безопасность применения комплексного противопаразитарного препарата, содержащего ивермектин и празиквантел, при различных формах паразитарных болезней крупного рогатого скота.
Материалы и методы. Исследование проводили в фермерском хозяйстве Калининградской области с 29 июля по 14 октября 2024 г. Из 890 голов крупного рогатого скота для эксперимента были отобраны 50 телок в возрасте 8–14 мес. с диагностированными нематодозами, цестодозами, трематодозами, арахнозами и энтомозами. Животные были разделены на пять групп в соответствии с видом инвазии. Препарат применяли перорально с кормом или заменителем молока в дозах, соответствующих массе тела и типу болезни. Диагностические мероприятия включали клинический осмотр, копрологические исследования (Фюллеборн, Щербович), ларвоскопию, микроскопию соскобов кожи и визуальную оценку.
Результаты и обсуждение. Использованные ранее методы показали полное устранение нематодозов и цестодозов при двукратном применении препарата, эффективность при арахнозах и энтомозах составила 80–90%. Препарат не вызывал побочных эффектов. Таким образом, комплексное средство, сочетающее ивермектин и празиквантел, является эффективным и безопасным для применения в ветеринарной практике и может использоваться для лечения и профилактики множественных паразитарных инвазий у крупного рогатого скота.
ФАРМАКОЛОГИЯ, ТОКСИКОЛОГИЯ
Цель исследований – изучение переносимости повышенных доз лекарственного препарата «Д-цифенотрин Комбо» (D-цифенотрин, пирипроксифен и пиперонилбутоксид) в форме раствора для наружного применения при обработке крупного рогатого скота разного возраста.
Материалы и методы. Во ВНИИП – филиале ФГБНУ ФНЦ ВИЭВ РАН был разработан препарат в форме раствора (концентрат) для наружного применения на основе трех активных компонентов: D-цифенотрина, пирипроксифена и пиперонилбутоксида для крупного рогатого скота, лошадей, овец при эктопаразитарных болезнях. Исследования проводили в июне и июле 2025 года в Москве и хозяйстве Карачаево-Черкесской Республики на клинически здоровых бычках и разнополом ремонтном молодняке крупного рогатого скота голштинской породы. Для обработки животных препарат применяли однократно индивидуально путем среднеобъемного опрыскивания 0,005%-ной водной эмульсией в дозе 12,5 мл на 1 кг массы тела (пятикратно увеличенная терапевтическая доза); животных контрольной группы не обрабатывали. До применения препарата и через 5 сут после обработки животных взвешивали, измеряли температуру тела, брали пробы крови для исследования некоторых морфологических и биохимических показателей по общепринятым методикам.
Результаты и обсуждение. Установлено, что исследуемый препарат при однократной обработке кожно-шерстного покрова животных в пятикратно увеличенной дозе в течение экспериментального периода не оказал отрицательного влияния на их общее состояние, физиологический статус и поведение. Не отмечено статистически значимых изменений морфологических и биохимических показателей крови у крупного рогатого скота из опытных групп по сравнению с контролем.
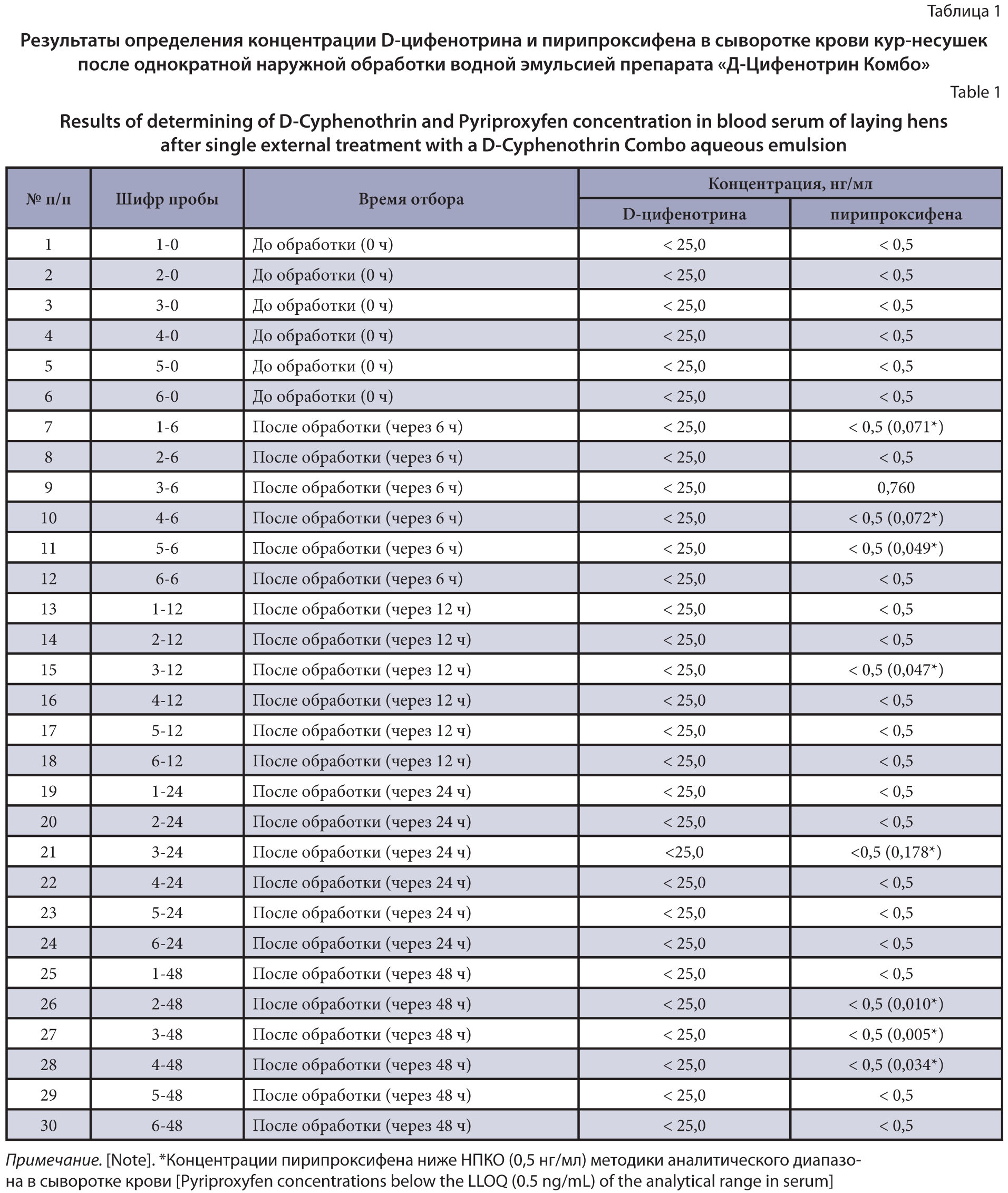
Цель исследований – определить остаточные количества D-цифенотрина и пирипроксифена в сыворотке крови и яйцах от кур-несушек до и после их наружной обработки водной эмульсией инсектоакарицидного средства «Д-цифенотрин Комбо».
Материалы и методы. Шесть кур-несушек кросса «СП-789» содержали индивидуально в клетках. Отбирали у них пробы крови до обработки и через 6, 12, 24, 48 ч после нее; проводили сбор яиц до и в течение 5 сут после обработки, которую осуществляли мелкокапельно 0,005%-ной водной эмульсией препарата «Д-цифенотрин Комбо». Концентрацию D-цифенотрина и пирипроксифена в пробах определяли с помощью жидкостной хроматографии/ масс-спектрометрии (LCMS), используя хромато-масс-спектрометрическую систему Shimadzu LCMS-8050 и другое лабораторное оборудование. Нижний предел количественного определения (НПКО) для D-цифенотрина в сыворотке крови кур составил 25,0 нг/мл, в яйце – 25,0 нг/г и НПКО пирипроксифена в сыворотке крови 0,5 нг/мл и в яйце – 0,5 нг/г.
Результаты и обсуждение. У одной курицы через 6 ч после обработки в сыворотке крови определена концентрация пирипроксифена выше НПКО – 0,760 нг/мл. Во всех остальных пробах, полученных от яичных кур кросса «СП-789», концентрации D-цифенотрина и пирипроксифена были ниже НПКО. Поэтому можно предположить об отсутствии ограничений по использованию яиц в пищевых целях после наружного применения цифенотрин и пирипроксифен содержащего препарата. Пиперонилбутоксид, входящий в состав препарата «Д-цифенотрин Комбо», не определяли методом LCMS в связи с особенностями его химического строения. Учитывая состав препарата, количественное содержание его компонентов, порядок применения (только наружное), данные нормативных документов, превышения пиперонилбутоксида в продуктах питания не предполагается. Исходя из вышеизложенного, ограничения по использованию яиц от кур после наружной обработки 0,005%-ной водной эмульсией исследуемого препарата в пищевых целях отсутствуют.
ПАМЯТИ УЧЕНОГО
ISSN 2541-7843 (Online)